știință > Chimie > coloizi> prepararea coloizilor
în acest articol, vom studia diferite metode de preparare a coloizilor.
prepararea solurilor Liofile:
pentru prepararea solurilor liofile, faza dispersată se adaugă direct în mediul de dispersie la rece sau prin încălzire.
soluții coloidale de amidon, lipici, gelatină etc. în apă pot fi preparate prin această metodă. Soluțiile de electroliți coloidali, cum ar fi săpunurile și coloranții, pot fi, de asemenea, preparate prin această metodă.
prepararea solurilor Liofobe:
pentru prepararea solurilor liofobe, substanța în vrac este descompusă în particule de dimensiuni coloidale (dispersie) sau agregând particule mai mici în particule de dimensiuni coloidale (condensare). Pentru a îmbunătăți stabilitatea sol anumite substanțe sunt adăugate la sol, substanțele adăugate se numesc stabilizatori.
metode de dispersie:
în metoda de dispersie, particulele de dimensiuni mai mari sunt defalcate la dimensiunea coloidală în mediul de dispersie. Începând cu materialul în formă masivă, se prepară o soluție coloidală utilizând dispozitive adecvate pentru dezintegrarea acestuia în particule de dimensiuni coloidale. În mod normal, acest lucru se realizează prin metode fizice.
metoda de dispersie Mecanică :
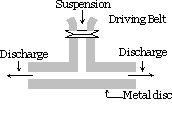
substanța care urmează să fie dispersată este măcinată fin. Apoi se amestecă cu mediul de dispersie, se adaugă și materiale de protecție sau stabilizator atunci când se obține o suspensie grosieră. Această suspensie este apoi trecută printr-o moară coloidă. O moară coloidă este formată din două discuri de metale grele plasate una deasupra celeilalte separate printr-un spațiu foarte mic unul de celălalt. Acestea sunt rotite în direcții opuse la o viteză foarte mare de aproximativ 7000 r.p.m. rezultatele sol datorită efectului mare de forfecare. Materialul de protecție utilizat previne coagularea particulelor.
folosind această metodă sols de indigo, sulf, pastă de dinți, cerneală de imprimantă, vopsele, unguente etc. sunt pregătite.
dispersie electrică sau metoda arcului lui Bredig:
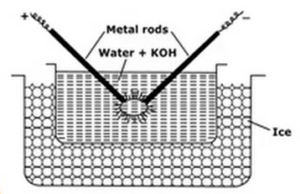
această metodă utilizată pentru sols metalice preparate cum ar fi platină, argint, aur, cupru în apă. Un mediu de dispersie (apă conductivă) și o urmă de hidroxid de sodiu (agentul stabilizator) sunt prelevate în vasul de porțelan sau sticlă (neconductor). Vasul care conține mediu de dispersie este înconjurat de un amestec de îngheț. Metalul care trebuie dispersat este scufundat în vas sub formă de electrozi. Electrozii sunt conectați la sursa de înaltă tensiune. Capetele electrozilor din mediul de dispersie sunt foarte apropiate unul de celălalt. Se aplică o tensiune foarte mare și apoi se lovește un arc electric între vârfurile electrozilor. Acest lucru creează căldură mare datorită căreia tijele metalice se topesc, se evaporă și se răcesc brusc datorită amestecului de înghețare dă naștere soluției coloidale a metalului.
funcțiile amestecurilor de congelare sunt
- amestecul de congelare ajută la condensarea vaporilor de metal care formează coloizii
- previne vaporizarea apei.
- previne coagularea coloizilor, prin menținerea sol rece.
Peptizare sau dispersie chimică:
Redispersia precipitatului proaspăt preparat în sol prin adăugarea unui electrolit care conține ion comun se numește peptizare. Un electrolit utilizat pentru peptizare este numit ca agent peptizant. Peptizarea este un proces invers de coagulare. Acțiunea de peptizare se datorează adsorbției preferențiale a unuia dintre ionii electrolitului pe precipitat.
Exemplul – 1:
precipitat Fe(OH)3 proaspăt preparat când este tratat cu soluție diluată de FeCl3, se formează hidroxid feric brun roșiatic sol (Fe3+ fiind Ion comun). În acest caz, FeCl3 este agentul peptizant.
Fe (OH)3 + FeCl3 Colosu Fe3+
exemplu – 2:
precipitat de clorură de argint proaspăt când este tratat cu o cantitate mică de HCl diluat, se formează un sol de clorură de argint.
exemplu – 3:
sulfatul de cadmiu poate fi peptizat cu ajutorul sulfatului de hidrogen.
dispersie cu ultrasunete:
ultrasunete este o metodă de procesare foarte eficientă în generarea și aplicarea particulelor de dimensiuni coloidale. Undele ultrasonice de înaltă intensitate sunt utilizate în acest scop. În timpul Sonicare de lichide undele ultrasonice care se propagă prin rezultat mediu de dispersie în alternarea de înaltă presiune (compresie) și joasă presiune (rarefiere) cicluri. Acest stres mecanic provoacă cavitație cu ultrasunete în lichide. Creează jeturi lichide de mare viteză de până la 1000 km/h. Astfel de jeturi presează lichidul la presiune ridicată între particule și le separă una de cealaltă. Particulele mai mici sunt accelerate cu jeturile de lichid și se ciocnesc la viteze mari.
diverse substanțe precum uleiurile, mercurul, sulful, sulfurile și oxizii metalelor pot fi dispersate în stare coloidală prin această metodă.
metode de condensare:
aceste metode implică reacții chimice. În aceste metode factori cum ar fi temperatura, presiunea, concentrațiile. etc. sunt întreținute corespunzător. Ionii nedoriți prezenți în sol sunt îndepărtați prin dializă , deoarece acești ioni pot coagula în cele din urmă solul.
metode chimice:
metoda de oxidare:
prepararea sulfului coloidal:
când H2S în apă (soluție apoasă) este expus la aer, se oxidează încet la sulf. Sulful astfel format rămâne în apă în stare coloidală, iar soluția astfel formată rămâne în apă în stare coloidală, iar soluția are un aspect ușor lăptos.
H2S + O2 H2O + 2s (coloidal)
un sol de sulf poate fi preparat și atunci când gazul H2S este barbotat printr-o soluție apoasă de SO2.
H2S + SO2 2 H2O + 3S (coloidal)
metoda de reducere:
prepararea aurului Sol:
un număr de metale precum argintul, aurul, platina, plumbul de mercur pot fi obținute în stare coloidală prin reducerea soluțiilor lor de sare (diluate) folosind agenți reducători adecvați precum hidrogen sulfurat, formaldehidă, clorură stanoasă, acid tanic etc.
sol auriu poate fi obținut atunci când soluția AuCl3(dil) este tratată cu clorură stanoasă.
2 AuCl3 + 3 SnCl2 3 Sncl4 + 2 au (coloidal)
în mod similar, se prepară soli cu mercur de argint, platină.
AgNO3 + acid tanic category: AG sol
Ascl3 + acid tanic category: au sol
metoda de hidroliză:
prepararea hidroxidului feric Sol:
se obține o soluție coloidală de hidroxid feric prin fierberea unei soluții diluate de clorură ferică.
FeCl3 + 3H2O fe(OH) 3 + 3 HCl
prepararea acidului Silicic Sol:
prin hidroliza unei soluții diluate de silicat de sodiu cu un acid clorhidric, se obține soluția coloidală de acid silicic.
metoda de descompunere dublă:
prepararea sulfurii Arsenioase Sol:
sulfura Arsenioasă, As2S3 este un coloid liofob. Se obține prin hidroliza oxidului arsenios (AS203) cu apă distilată clocotită, urmată de trecerea gazului H2S prin soluția obținută. În soluția coloidală de sulfură arsenioasă, fiecare particulă este înconjurată de ioni HS, produși prin disocierea H2S. Acest strat de ioni de sulfură este înconjurat în continuare de stratul de ioni de ioni H+.
As2O3 + 3 H2O 2AS(OH)3 (fierbere)
2 As(OH)3 + 3h2s as2s3 + 6h2o
(sol galben deschis)
prin metoda solventului de schimb:
există o serie de substanțe ale căror soluții coloidale pot fi preparate soluția substanței într-un solvent și turnarea acesteia într-un alt solvent în care substanța este relativ mai puțin solubilă.
prepararea sulfului sau a fosforului Sol:
dacă o soluție de sulf sau fosfor preparată în alcool este turnată în apă, se obține o soluție coloidală de sulf sau fosfor datorită solubilității scăzute a sulfului sau fosforului în apă.
prin schimbarea stării fizice:
o soluție coloidală a anumitor elemente, cum ar fi mercurul și sulful, se obține prin trecerea vaporilor lor prin apă rece care conține un stabilizator ( o sare de amoniu sau un citrat).
Metoda De Răcire Excesivă:
o soluție coloidală de gheață într-un solvent organic cum ar fi eter sau cloroform poate fi preparată prin înghețarea unei soluții de apă în solvent. Moleculele de apă care nu mai pot fi ținute în soluție, se combină separat pentru a forma particule de dimensiuni coloidale.
purificarea soluției coloidale
dializă:
procesul de separare a particulelor de coloid de cele ale cristaloidului, prin difuzie printr-o membrană adecvată (membrană animală sau hârtie pergament) se numește dializă. Aparatul utilizat pentru efectuarea dializei se numește dializor.
principiu:
particulele coloidale nu pot trece printr-o membrană pergament sau celofan în timp ce ionii electrolitului (cristaloizi) pot trece prin ea.
procedeu:
o pungă formată din membrană semipermeabilă adecvată care conține soluția coloidală este suspendată într-un vas prin care se circulă continuu apă proaspătă. Moleculele și ionii de cristaloizi difuzează prin membrană în apă și sunt spălați. Astfel, solul din pungă este purificat.
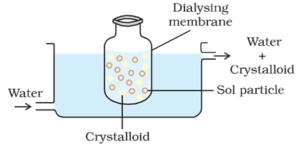
dializa poate fi utilizată pentru îndepărtarea HCl din hidroxidul feric sol.
electrodializă:
procesul obișnuit de dializă este lent. (ii) pentru a crește procesul de purificare, dializa se efectuează prin aplicarea unui câmp electric. Acest proces se numește electrodializă. Ionii prezenți în soluția coloidală migrează spre electrozi încărcați opus.

aplicarea importantă a procesului de electrodializă în aparatul de rinichi artificial utilizat pentru purificarea sângelui pacienților ai căror rinichi nu au reușit să funcționeze.
ultrafiltrare:
porii hârtiei de filtru obișnuite sunt mari, prin urmare particulele coloidale trec prin ele cu ușurință. Dacă porii hârtiei de filtru obișnuite sunt micșorați prin înmuierea hârtiei de filtru într-o soluție de gelatină de coloidion (este un amestec de nitro-celuloză 4% în alcool și eter) și ulterior întăriți prin înmuierea în formaldehidă
hârtia de filtru tratată poate reține particulele coloidale și permite scăparea particulelor soluției adevărate. O astfel de hârtie de filtru este cunoscută sub numele de ultrafilter, iar procesul de separare a coloizilor prin utilizarea ultrafilterelor este cunoscut sub numele de ultrafiltrare.
particulele coloidale rămase pe hârtia ultrafilter sunt apoi spălate cu un mediu de dispersie proaspăt pentru a obține o soluție coloidală pură.
ultracentrifugare:
în această metodă, soluția coloidală este plasată într-o mașină centrifugă de mare viteză. La centrifugare, particulele coloidale se așează. Impuritățile rămân în centrifugat și sunt îndepărtate. Particulele coloidale decontate sunt amestecate cu mediul de dispersie pentru a forma din nou soluția coloidală.