videnskab > Kemi > kolloider > fremstilling af kolloider
i denne artikel skal vi studere forskellige metoder til fremstilling af kolloider.
fremstilling af lyofile Soler:
til fremstilling af lyofil sol tilsættes den dispergerede fase direkte til dispersionsmediet i kulde eller ved opvarmning.
kolloide opløsninger af stivelse, lim, gelatine osv. i vand kan fremstilles ved denne metode. Opløsninger af kolloide elektrolytter såsom sæber og farvestoffer kan også fremstilles ved denne metode.
fremstilling af Lyofobe Soler:
til fremstilling af lyofob sol nedbrydes stoffet i bulk i partikler med kolloide dimensioner (Dispersion) eller aggregerer mindre partikler i partikler med kolloide dimensioner (kondensation). For at forbedre stabiliteten af sol tilsættes visse stoffer til sol, de tilsatte stoffer kaldes stabilisatorer.
Dispersionsmetoder:
i dispersionsmetoden nedbrydes partikel af større størrelse til den kolloide størrelse i dispersionsmediet. Begyndende med materialet i massiv form fremstilles en kolloid opløsning ved anvendelse af egnede indretninger til at nedbryde det i partikler af kolloid størrelse. Normalt udføres dette ved fysiske metoder.
mekanisk dispersionsmetode :
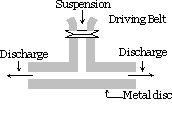
det stof, der skal dispergeres, er finmalet. Det blandes derefter med dispersionsmediet, beskyttelsesmaterialer eller stabilisator tilsættes også, når der opnås en grov suspension. Denne suspension føres derefter gennem en kolloidmølle. En kolloidmølle består af to tungmetalskiver placeret oven over hinanden adskilt af et meget lille hul fra hinanden. De drejes i modsatte retninger med en meget høj hastighed på omkring 7000 r.p.m. sol resultater på grund af den store klipning effekt. Anvendt beskyttelsesmateriale forhindrer partikler i koagulering.
brug af denne metode sols af indigo, svovl, tandpasta, printerblæk, maling, salver osv. er forberedt.
elektrisk Dispersion eller Bredig ‘ s Arc-metode:
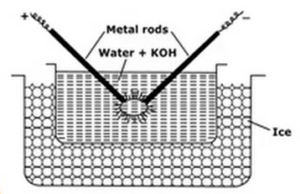
denne metode bruges til at fremstille metal Soler som platin, sølv, guld, kobber i vand. Et dispersionsmedium (ledningsevne vand) og et spor af natriumhydroksid (stabiliseringsmidlet) tages i porcelæn eller glas (ikke ledende) beholder. Beholderen indeholdende dispersionsmedium er omgivet af en fryseblanding. Metal, der skal dispergeres, dyppes i beholderen i form af elektroder. Elektroder er forbundet til højspændingskilden. Enderne af elektroder i dispersionsmediet er meget tæt på hinanden. En meget høj spænding påføres, og derefter rammes en elektrisk lysbue mellem elektrodernes spidser. Dette skaber stor varme på grund af hvilken metalstænger smelter, fordamper og pludselig afkøles på grund af fryseblanding giver anledning til den kolloide opløsning af metallet.
fryseblandingernes funktioner er
- Fryseblanding hjælper med kondensering af metaldampe, der danner kolloiderne
- det forhindrer fordampning af vand.
- det forhindrer koagulering af kolloider ved at holde sol kold.
peptisering eller kemisk Dispersion:
Redispersion af frisklavet bundfald i solen ved tilsætning af en elektrolyt indeholdende fælles ion kaldes som peptisering. En elektrolyt, der anvendes til peptisering, kaldes peptiseringsmidlet. Peptisering er en omvendt koagulationsproces. Peptiseringsvirkningen skyldes den præferentielle adsorption af en af ionerne af elektrolytten på bundfaldet.
eksempel – 1:
frisklavet Fe(OH)3 bundfald ved behandling med fortyndet opløsning af FeCl3 dannes rødbrun jernhydroksidsol (Fe3+ er almindelig ion). I dette tilfælde er FeCl3 peptiseringsmidlet.
Fe (OH)3 + FeCl3 liter Fe3+
eksempel – 2:
frisk sølvchloridfældning når der behandles med en lille mængde fortyndet HCl, dannes en sølvchloridsol.
eksempel – 3:
Cadmiumsulfat kan peptiseres ved hjælp af hydrogensulfat.
Ultralyddispersion:
ultralyd er en meget effektiv behandlingsmetode til generering og anvendelse af kolloide størrelsespartikler. Ultralydbølger med høj intensitet anvendes til dette formål. Under sonikering af væsker resulterer ultralydbølgerne, der formerer sig gennem dispersionsmedium, i skiftende højtrykscyklusser (kompression) og lavtrykscyklusser (rarefaction). Denne mekaniske belastning forårsager ultralydkavitation i væsker. Det skaber højhastigheds væskestråler på op til 1000 km/t. Sådanne stråler presser væske ved højt tryk mellem partiklerne og adskiller dem fra hinanden. Mindre partikler accelereres med væskestrålerne og kolliderer ved høje hastigheder.
forskellige stoffer som olier, kviksølv, svovl, sulfider og ilter af metal kan dispergeres i kolloid tilstand ved denne metode.
Kondensationsmetoder:
disse metoder involverer kemiske reaktioner. I disse metoder faktorer som temperatur, tryk, koncentrationer. osv. er korrekt vedligeholdt. De uønskede ioner , der er til stede i solen, fjernes ved dialyse, da disse ioner til sidst kan koagulere solen.
kemiske metoder:
iltning metode:
fremstilling af kolloid svovl:
når H2S i vand (vandig opløsning) udsættes for luft, bliver det langsomt iltet til svovl. Den således dannede svovl forbliver i vand i kolloid tilstand, og den således dannede opløsning forbliver i vand i kolloid tilstand, og opløsningen har et lidt mælkagtigt udseende.
H2S + O2 liter H2O + 2s (kolloid)
en svovlsol kan også fremstilles, når H2S-gas bObles gennem en vandig opløsning af SO2.
H2S + SO2 liter 2 H2O + 3s (kolloid)
reduktionsmetode:
fremstilling af Guldsol:
et antal metaller som sølv, guld, platin, kviksølvbly kan opnås i kolloid tilstand ved reduktion af deres saltopløsninger (fortyndet) ved anvendelse af egnede reduktionsmidler som hydrogensulfid, formaldehyd, stannouschlorid, tanninsyre osv.
Guld sol kan opnås, når AuCl3(dil) opløsning behandles med stannøst chlorid.
2 AuCl3 + 3 SnCl2 liter 3 SnCl4 + 2 Au (kolloid)
tilsvarende fremstilles sølv, platin kviksølvsoler.
AgNO3 + garvesyre-sol
AuCl3 + garvesyre-Sol
Hydrolysemetode:
fremstilling af Ferrihydroksid Sol:
en kolloid opløsning af ferrihydroksid opnås ved kogning af en fortyndet opløsning af ferrichlorid.
FeCl3 + 3H2O kurfee (OH) 3 + 3 HCl
fremstilling af kiselsyre Sol:
ved hydrolyse af en fortyndet opløsning af natriumsilicat med en saltsyre opnås den kolloide opløsning af kiselsyre.
Dobbelt Nedbrydningsmetode:
fremstilling af arsenisk sulfid Sol:
arsenisk sulfid, As2S3 er en lyofob kolloid. Det opnås ved hydrolyse af arsenisk ilt (AS203) med kogende destilleret vand efterfulgt af at føre H2S-gas gennem den opnåede opløsning. I den kolloide opløsning af arsenisk sulfid er hver partikel omgivet af HS – ioner, produceret ved dissociation af H2S. Dette sulfidionlag er yderligere omgivet af modionlaget af H+ ioner.
As2O3 + 3 H2O Lira 2AS(OH)3 (kogende)
2 As(OH)3 + 3H2S Lira As2S3 + 6H2O
(lysegul sol)
ved udveksling af Opløsningsmiddelmetode:
der er en række stoffer, hvis kolloide opløsninger kan fremstilles ved at tage en opløsning af stoffet i et opløsningsmiddel og hælde det i et andet opløsningsmiddel, hvor stoffet er relativt mindre opløseligt.
fremstilling af svovl-eller Fosforsol:
hvis en opløsning af svovl eller fosfor fremstillet i alkohol hældes i vand, opnås en kolloid opløsning af svovl eller fosfor på grund af den lave opløselighed af svovl eller fosfor i vand.
ved ændring af fysisk tilstand:
en kolloid opløsning af visse grundstoffer såsom kviksølv og svovl opnås ved at føre deres dampe gennem koldt vand indeholdende en stabilisator ( et ammoniumsalt eller et citrat).
Overdreven Kølemetode:
en kolloid opløsning af is i et organisk opløsningsmiddel som ether eller chloroform kan fremstilles ved frysning af en opløsning af vand i opløsningsmidlet. Vandmolekylerne, som ikke længere kan holdes i opløsning, kombineres separat for at danne partikler af kolloid størrelse.
oprensning af kolloid opløsning
dialyse:
processen med at adskille partiklerne af kolloid fra krystalloid ved hjælp af diffusion gennem en egnet membran (dyremembran eller pergamentpapir) kaldes dialyse. Apparatet, der anvendes til udførelse af dialyse, kaldes dialyser.
princip:
de kolloide partikler kan ikke passere gennem en pergament-eller cellofanmembran, mens ionerne af elektrolytten (krystalloider) kan passere gennem den.
proces:
en pose bestående af egnet semipermeabel membran indeholdende den kolloide opløsning suspenderes i en beholder, gennem hvilken ferskvand kontinuerligt flyves. Molekyler og ioner af krystalloider diffunderer gennem membranen i vandet og vaskes væk. Således renses solen i posen.
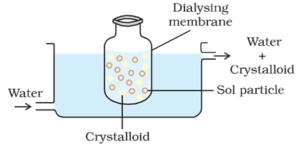
dialyse kan bruges til at fjerne HCl fra jernhydroksidsolet.
elektrodialyse:
den almindelige dialyseproces er langsom. (ii) for at øge rensningsprocessen udføres dialysen ved at anvende et elektrisk felt. Denne proces kaldes elektrodialyse. Ionerne, der er til stede i den kolloide opløsning, migrerer mod modsat ladede elektroder.

den vigtige anvendelse af elektrodialyse proces i den kunstige nyre maskine, der anvendes til rensning af blodet hos de patienter, hvis nyrer har undladt at arbejde.
ultrafiltrering:
porerne i almindeligt filterpapir er store, derfor passerer kolloide partikler let gennem dem. Hvis porerne i det almindelige filterpapir gøres mindre ved blødgøring af filterpapiret i en opløsning af gelatine af kolloidion (det er en blanding af 4% nitrocellulose i alkohol og ether) og derefter hærdes ved blødgøring i formaldehyd
kan det behandlede filterpapir tilbageholde kolloide partikler og lade de sande opløsningspartikler slippe ud. Et sådant filterpapir er kendt som ultrafilter, og processen med at adskille kolloider ved hjælp af ultrafiltre er kendt som ultrafiltrering.
de kolloide partikler, der er tilbage på ultrafilterpapir, vaskes derefter med et frisk dispersionsmedium for at få en ren kolloid opløsning.
ultracentrifugering:
i denne metode placeres den kolloide opløsning i en højhastighedscentrifugalmaskine. Ved centrifugering sætter de kolloide partikler sig ned. Urenhederne forbliver i centrifugatet og fjernes. De bundfældede kolloide partikler blandes med dispersionsmediet til dannelse af den kolloide opløsning igen.