vetenskap > Kemi > kolloider > beredning av kolloider
i denna artikel ska vi studera olika metoder för beredning av kolloider.
beredning av Lyofil Sol:
för beredning av lyofil sol tillsätts den dispergerade fasen direkt till dispersionsmedium i kyla eller genom uppvärmning.
kolloidala lösningar av stärkelse, lim, gelatin etc. i vatten kan beredas med denna metod. Lösningar av kolloidala elektrolyter såsom tvålar och färgämnen kan också framställas med denna metod.
beredning av lyofoba Soler:
för beredning av lyofob sol bryts ämnet i bulk ned i partiklar med kolloidala dimensioner (Dispersion) eller aggregerar mindre partiklar till partiklar med kolloidala dimensioner (kondensation). För att förbättra stabiliteten hos sol tillsätts vissa ämnen till sol, de tillsatta ämnena kallas stabilisatorer.
Dispersionsmetoder:
i dispersionsmetoden partikel av större storlek bryts ner till den kolloidala storleken i dispersionsmediet. Från och med materialet i massiv form framställs en kolloidal lösning genom användning av lämpliga anordningar för att sönderfalla den i partiklar av kolloidal storlek. Normalt utförs detta med fysiska metoder.
mekanisk dispersionsmetod :
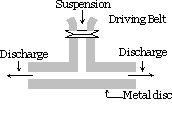
ämnet som ska dispergeras är finmalt. Det blandas sedan med dispersionsmediet, skyddande material eller stabilisator tillsätts också när en grov suspension erhålls. Denna suspension passeras sedan genom en kolloidkvarn. En kolloidkvarn består av två tungmetallskivor placerade ovanför varandra åtskilda av ett mycket litet gap från varandra. De roteras i motsatta riktningar med en mycket hög hastighet på cirka 7000 r.p.m. sol-resultaten på grund av den stora skjuvningseffekten. Skyddande material som används förhindrar partiklar från koagulering.
med denna metod sols av indigo, svavel, tandkräm, skrivare bläck, färger, salvor etc. är beredda.
elektrisk Dispersion eller Bredigs Bågmetod:
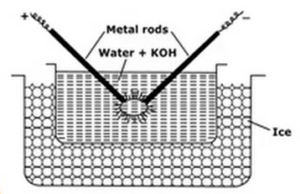
denna metod som används för att beredda metall sols som platina, silver, guld, koppar i vatten. Ett dispersionsmedium (konduktivitetsvatten) och ett spår av natriumhydroxid (stabiliseringsmedlet) tas i porslin eller glas (icke ledande) kärl. Kärlet som innehåller dispersionsmedium omges av en frysblandning. Metall som ska dispergeras doppas i kärlet i form av elektroder. Elektroder är anslutna till högspänningskällan. Ändarna av elektroder i dispersionsmediet är mycket nära varandra. En mycket hög spänning appliceras och sedan slås en elektrisk båge mellan elektrodernas spetsar. Detta skapar stor värme på grund av vilken metallstavar smälter, avdunstar och plötsligt kyls på grund av frysning blandningen ger upphov till den kolloidala lösningen av metallen.
funktionerna för frysblandningarna är
- Frysblandningen hjälper till att kondensera metallånga som bildar kolloiderna
- den förhindrar förångning av vatten.
- det förhindrar koagulering av kolloider genom att hålla sol kallt.
Peptisering eller kemisk Dispersion:
Redispersion av nyberedd fällning i sol genom tillsats av en elektrolyt innehållande vanlig Jon kallas peptisering. En elektrolyt som används för peptisering kallas som peptiseringsmedlet. Peptisering är en omvänd koagulationsprocess. Peptiseringsverkan beror på preferensadsorptionen av en av jonerna i elektrolyten på fällningen.
exempel-1:
nyberedd Fe(OH)3 fällning vid behandling med utspädd lösning av FeCl3 bildas rödbrun järnhydroxidsol (Fe3+ är vanlig Jon). I detta fall är FeCl3 peptiseringsmedlet.
Fe (OH)3 + FeCl3 Occloritis Fe3+
exempel – 2:
färsk silverkloridfällning vid behandling med en liten mängd utspädd HCl bildas en silverkloridsol.
exempel-3:
Kadmiumsulfat kan peptiseras med hjälp av vätesulfat.
Ultraljudsdispersion:
ultraljud är en mycket effektiv bearbetningsmetod vid generering och applicering av kolloidala partiklar. Högintensiva ultraljudsvågor används för detta ändamål. Under sonicating av vätskor ultraljud vågor som förökar sig genom dispersion medium resulterar i alternerande högtrycks (kompression) och lågtrycks (rarefaction) cykler. Denna mekaniska stress orsakar ultraljudskavitation i vätskor. Det skapar höghastighetsvätskestrålar på upp till 1000 km/h. Sådana strålar pressar vätska vid högt tryck mellan partiklarna och separerar dem från varandra. Mindre partiklar accelereras med vätskestrålarna och kolliderar vid höga hastigheter.
olika ämnen som oljor, kvicksilver, svavel, sulfider och oxider av metall kan dispergeras i kolloidalt tillstånd med denna metod.
Kondenseringsmetoder:
dessa metoder innefattar kemiska reaktioner. I dessa metoder faktorer som temperatur, tryck, koncentrationer. osv. underhålls ordentligt. De oönskade joner som finns i sol avlägsnas genom dialys, eftersom dessa joner så småningom kan koagulera sol.
kemiska metoder:
Oxidationsmetod:
beredning av kolloidalt svavel:
när H2S i vatten (vattenlösning) utsätts för luft oxideras det långsamt till svavel. Det svavel som bildas på detta sätt förblir i vatten i kolloidalt tillstånd och lösningen som bildas på detta sätt förblir i vatten i kolloidalt tillstånd och lösningen har ett något mjölkigt utseende.
H2S + O2 oz. H2o + 2s (kolloidal)
en sol av svavel kan också beredas när h2s-gas bubblas genom en vattenlösning av SO2.
H2S + SO2 2H2O + 3S (kolloidal)
Reduktionsmetod:
framställning av guld Sol:
ett antal metaller som silver, guld, platina, kvicksilver bly kan erhållas i kolloidalt tillstånd genom reduktion av deras saltlösningar (utspädd) med användning av lämpliga reduktionsmedel som vätesulfid, formaldehyd, stannös klorid, garvsyra etc.
Gold sol kan erhållas när AuCl3(dil) lösning behandlas med stannös klorid.
2 AuCl3 + 3 SnCl2 1cl4 + 2 2CL (kolloidal)
på liknande sätt framställs silver, platina kvicksilver Soler.
AgNO3 + garvsyra 2G ag sol
AuCl3 + garvsyra 2G au sol
Hydrolysmetod:
beredning av järnhydroxid Sol:
en kolloidal lösning av järnhydroxid erhålls genom kokning av en utspädd lösning av järnklorid.
FeCl3 + 3H2O ci fe(OH)3 + 3 HCl
beredning av kiselsyra Sol:
genom hydrolys av en utspädd lösning av natriumsilikat med en saltsyra erhålles den kolloidala lösningen av kiselsyra.
Dubbel Sönderdelningsmetod:
beredning av Arsenisk Sulfidsol:
Arsenisk sulfid, As2S3 är en lyofob kolloid. Det erhålls genom hydrolys av arsenikoxid (AS203) med kokande destillerat vatten, följt av att passera H2S-gas genom den erhållna lösningen. I den kolloidala lösningen av arsenisk sulfid omges varje partikel av HS-joner, som produceras genom dissociation av H2S. Detta sulfidjonskikt omges vidare av motjonskiktet av H+ – joner.
As2O3 + 3 H2o 2AS(OH)3 (kokande)
2 As(OH)3 + 3h2s 2s a2s3 + 6h2o
(ljusgul sol)
genom utbyte av Lösningsmedelsmetod:
det finns ett antal ämnen vars kolloidala lösningar kan framställas genom att ta en lösning lösning av ämnet i ett lösningsmedel och häll det i ett annat lösningsmedel där ämnet är relativt mindre lösligt.
beredning av svavel-eller Fosforsol:
om en lösning av svavel eller fosfor framställd i alkohol hälls i vatten, erhålls en kolloidal lösning av svavel eller fosfor på grund av den låga lösligheten av svavel eller fosfor i vatten.
genom förändring av fysikaliskt tillstånd:
en kolloidal lösning av vissa ämnen såsom kvicksilver och svavel erhålls genom att deras ångor passerar genom kallt vatten innehållande en stabilisator ( ett ammoniumsalt eller ett citrat).
Överdriven Kylmetod:
en kolloidal lösning av IS i ett organiskt lösningsmedel som eter eller kloroform kan framställas genom frysning av en lösning av vatten i lösningsmedlet. Vattenmolekylerna som inte längre kan hållas i lösning kombineras separat för att bilda partiklar av kolloidal storlek.
rening av kolloidal lösning
dialys:
processen att separera kolloidpartiklarna från kristalloidpartiklarna genom diffusion genom ett lämpligt membran (djurmembran eller pergamentpapper) kallas dialys. Apparaten som används för att utföra dialys kallas dialyser.
princip:
de kolloidala partiklarna kan inte passera genom ett pergament eller cellofanmembran medan jonerna i elektrolyten (kristalloiderna) kan passera genom den.
Process:
en påse bestående av lämpligt semipermeabelt membran innehållande den kolloidala lösningen suspenderas i ett kärl genom vilket färskvatten kontinuerligt flögs. Molekylerna och jonerna av kristalloider diffunderar genom membranet i vattnet och tvättas bort. Således renas sol i påsen.
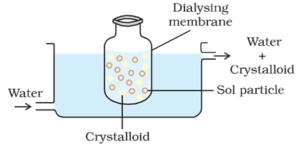
dialys kan användas för att avlägsna HCl från järnhydroxidsolen.
elektrodialys:
den vanliga dialysprocessen är långsam. (ii) för att öka reningsprocessen utförs dialysen genom att applicera ett elektriskt fält. Denna process kallas elektrodialys. De joner som finns i den kolloidala lösningen migrerar mot motsatt laddade elektroder.

den viktiga tillämpningen av elektrodialysprocessen i den konstgjorda njurmaskinen som används för rening av blodet hos de patienter vars njurar inte har fungerat.
ultrafiltrering:
porerna i vanligt filterpapper är stora, varför kolloidala partiklar lätt passerar genom dem. Om porerna i det vanliga filterpapperet görs mindre genom blötläggning av filterpapperet i en lösning av gelatin av kolloidion (det är en blandning av 4% nitrocellulosa i alkohol och eter) och därefter härdas genom blötläggning i formaldehyd
kan det behandlade filterpapperet behålla kolloidala partiklar och låta de verkliga lösningspartiklarna Fly. Sådant filterpapper är känt som ultrafilter och processen att separera kolloider med hjälp av ultrafilter kallas ultrafiltrering.
de kolloidala partiklarna kvar på ultrafilterpapper tvättas sedan med ett nytt dispersionsmedium för att få en ren kolloidal lösning.
ultracentrifugering:
i denna metod placeras den kolloidala lösningen i en höghastighets centrifugalmaskin. Vid centrifugering sätter de kolloidala partiklarna sig ner. Föroreningarna förblir i centrifugatet och avlägsnas. De sedimenterade kolloidala partiklarna blandas med dispersionsmediet för att bilda den kolloidala lösningen igen.