tiede > kemia > kolloidien valmistus > kolloidien valmistus
tässä artikkelissa tutkitaan erilaisia kolloidien valmistusmenetelmiä.
Lyofiilisen Solin valmistus:
lyofiilisen Solin valmistamiseksi dispergoitunut faasi lisätään suoraan dispersioaineeseen kylmässä tai lämmittämällä.
kolloidiset liuokset tärkkelystä, liimaa, liivatetta jne. vedessä voidaan valmistaa tällä menetelmällä. Tällä menetelmällä voidaan valmistaa myös kolloidisten elektrolyyttien, kuten saippuoiden ja väriaineiden liuoksia.
Lyofobisen Solin valmistaminen:
lyofobisen Solin valmistaminen: irtotavarana oleva aine hajotetaan kolloidisiksi hiukkasiksi (dispersio) tai kootaan pienemmät hiukkaset kolloidisiksi hiukkasiksi (kondensaatio). SOL: n stabiilisuuden parantamiseksi sol: iin lisätään tiettyjä aineita, lisättyjä aineita kutsutaan stabilointiaineiksi.
Dispersiomenetelmät:
dispersiomenetelmässä isokokoiset partikkelit hajoavat kolloidiseen kokoon dispersioväliaineessa. Massiivisessa muodossa olevasta materiaalista valmistetaan kolloidinen liuos sopivilla laitteilla sen hajottamiseksi kolloidisiksi hiukkasiksi. Yleensä tämä suoritetaan fysikaalisin menetelmin.
mekaaninen dispersiomenetelmä :
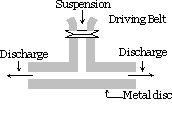
hajotettava aine jauhetaan hienoksi. Sen jälkeen se sekoitetaan dispersioväliaineen kanssa, suojamateriaaleja tai stabilointiainetta lisätään myös, kun saadaan karkea suspensio. Suspensio johdetaan kolloidimyllyn läpi. Kolloidimylly koostuu kahdesta raskasmetallilevystä, jotka on asetettu toisen yläpuolelle ja erotettu toisistaan hyvin pienellä raolla. Niitä pyöritetään vastakkaisiin suuntiin erittäin suurella nopeudella noin 7000 r. p. m. sol tulokset johtuen suuri leikkaus vaikutus. Käytetty suojamateriaali ehkäisee hiukkasten hyytymistä.
tätä menetelmää käyttäen sols indigoa, rikkiä, hammastahnaa,tulostinmustetta, maaleja, voiteita jne. olemme valmiita.
sähköinen dispersio eli Bredigin Kaarimenetelmä:
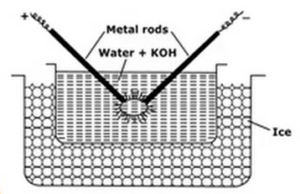
tätä menetelmää käytetään valmisteltaessa metalli sols kuten platina, hopea, kulta, kupari vedessä. Dispersioaine (johtavuusvesi) ja natriumhydroksidin (stabilointiaine) jäämä otetaan posliiniseen tai lasiseen (johtamattomaan) astiaan. Dispersioainetta sisältävän astian ympärillä on jäätävä seos. Dispergoitava metalli kastetaan astiaan elektrodien muodossa. Elektrodit on kytketty suurjännitelähteeseen. Dispersioväliaineen elektrodien päät ovat hyvin lähellä toisiaan. Käytetään erittäin suurta jännitettä ja sitten elektrodien kärkien väliin isketään valokaari. Näin syntyy suuri lämpö, jonka vuoksi metallitangot sulavat, haihtuvat ja jäätymisen vuoksi äkillisesti jäähtynyt seos synnyttää metallin kolloidisen liuoksen.
jäätymisseosten funktiot ovat
- Jäätymisseos auttaa kolloideja muodostavien metallihöyryjen tiivistymisessä
- se estää veden höyrystymisen.
- se estää kolloidien hyytymistä pitämällä Solin kylmänä.
Peptisointi tai Kemiallinen dispersio:
vastavalmistetun saostuman uudelleensyntymistä Soliin lisäämällä tavallista Ionia sisältävää elektrolyyttiä kutsutaan peptisoinniksi. Peptisointiin käytettävää elektrolyyttiä kutsutaan peptisoivana aineena. Pepitaatio on käänteinen hyytymisprosessi. Peptisointivaikutus johtuu elektrolyytin yhden ionin etuoikeutetusta adsorptiosta saostumaan.
Esimerkki-1:
vastavalmistettu Fe(OH)3-sakka, kun sitä käsitellään laimealla fecl3-liuoksella, muodostuu punaruskeaa ferrihydroksidisolia (Fe3+ on yhteinen ioni). Tässä tapauksessa fecl3 on peptisoiva aine.
Fe (OH)3 + Fecl3 → Fe3+
Esimerkki – 2:
tuore Hopeakloridisaostuma, kun sitä käsitellään pienellä määrällä laimeaa HCl: ää, muodostuu hopeakloridisolia.
esimerkki-3:
Kadmiumsulfaattia voidaan peptisoida vetysulfaatin avulla.
Ultraäänidispersio:
ultraääni on erittäin tehokas käsittelymenetelmä kolloidisten kokohiukkasten tuottamisessa ja levittämisessä. Tähän tarkoitukseen käytetään korkean intensiteetin ultraääniaaltoja. Nesteiden sonikoinnin aikana dispersiovälineen kautta etenevät ultraääniaallot johtavat vuorotteleviin korkeapaine-(puristus) ja matalapaine-(rarefaction) sykleihin. Tämä mekaaninen rasitus aiheuttaa nesteissä Ultraäänikavitaatiota. Se luo nopeita nestesuihkuja jopa 1000km / h. Tällaiset suihkut puristavat nestettä korkeassa paineessa hiukkasten välillä ja erottavat ne toisistaan. Pienemmät hiukkaset kiihtyvät nestesuihkuilla ja törmäävät toisiinsa suurilla nopeuksilla.
erilaiset aineet, kuten öljyt, elohopea, rikki, sulfidit ja metallioksidit, voidaan hajottaa kolloidisessa tilassa tällä menetelmällä.
Kondensaatiomenetelmät:
näihin menetelmiin liittyy kemiallisia reaktioita. Näissä menetelmissä tekijät, kuten lämpötila, paine, pitoisuudet. jne. huolletaan asianmukaisesti. Sol: ssä olevat ei-toivotut ionit poistetaan dialyysillä , sillä nämä ionit saattavat lopulta hyytyä sol: iin.
kemialliset menetelmät:
hapetusmenetelmä:
kolloidisen rikin valmistus:
kun H2S vedessä (vesiliuoksessa) altistuu ilmalle, se hapettuu hitaasti rikiksi. Näin muodostunut rikki jää veteen kolloidisessa tilassa ja näin muodostunut liuos jää veteen kolloidisessa tilassa ja liuos on hieman maitomainen.
H2S + O2 → H2o + 2s (kolloidinen)
solia rikkiä voidaan valmistaa myös, kun H2S-kaasua kuplitetaan SO2: n vesiliuoksen läpi.
H2S + SO2 → 2 H2O + 3S (kolloidinen)
Pelkistysmenetelmä:
Kullanvalmistus:
useita metalleja, kuten hopeaa, kultaa, platinaa, elohopea lyijyä, voidaan saada kolloidisessa tilassa pelkistämällä niiden suolaliuoksia (laimeita) käyttämällä sopivia pelkistäviä aineita, kuten rikkivetyä, formaldehydiä, tinakloridia, parkkihappoa jne.
Kultasuolta saadaan, kun aucl3(dil) – liuosta käsitellään tinakloridilla.
2 AuCl3 + 3 SnCl2 → 3 SnCl4 + 2 Au (kolloidinen)
samoin valmistetaan hopea-ja platinaelohopeaa.
AgNO3 + parkkihappo → AG sol
aucl3 + parkkihappo → Au sol
Hydrolyysimenetelmä:
Rautahydroksidin valmistus Sol:
kolloidinen rautahydroksidiliuos saadaan keittämällä laimeaa rautakloridiliuosta.
FeCl3 + 3H2O → Fe (OH) 3 + 3 HCl
Piihappoliuoksen valmistus:
laimean natriumsilikaattiliuoksen hydrolyysillä kloorivetyhapolla saadaan piihapon kolloidinen liuos.
Kaksoishajoamismenetelmä:
Arsenisulfidivalmiste Sol:
Arsenisulfidi, As2S3 on kylmäkammoinen kolloidi. Sitä saadaan hydrolysoimalla arseenioksidia (AS203) kiehuvalla tislatulla vedellä, minkä jälkeen H2S-kaasu johdetaan saadun liuoksen läpi. Arseenisulfidin kolloidisessa liuoksessa jokaista hiukkasta ympäröivät HS-ionit, joita syntyy H2S: n dissosioituessa. Tätä sulfidi-ionikerrosta ympäröi edelleen H+ – ionien vasta-ionikerros.
As2O3 + 3 H2O → 2AS(OH)3 (Kiehuva)
2 As(OH)3 + 3H2S → As2S3 + 6H2O
(vaaleankeltainen sol)
Vaihtoliuotusmenetelmällä:
on olemassa useita aineita, joiden kolloidisia liuoksia voidaan valmistaa ottamalla aineen liuos yhdessä liuottimessa ja sen kaataminen toiseen liuottimeen, johon aine liukenee suhteellisesti vähemmän.
rikki-tai Fosforivalmiste Sol:
jos veteen kaadetaan alkoholissa valmistettua rikki-tai fosforiliuosta, saadaan rikkiä tai fosforia sisältävää kolloidista liuosta, koska rikki tai fosfori liukenee veteen heikosti.
fysikaalisen olomuodon muutoksella:
tietyistä alkuaineista, kuten elohopeasta ja rikistä, muodostuva kolloidinen liuos saadaan johtamalla niiden höyryt stabilointiainetta ( ammoniumsuolaa tai sitraattia) sisältävän kylmän veden läpi.
Liiallinen Jäähdytysmenetelmä:
orgaanisessa liuottimessa, kuten eetterissä tai kloroformissa, olevaa kolloidista jääliuosta voidaan valmistaa jäädyttämällä liuottimessa oleva vesiliuos. Veden molekyylit, joita ei voi enää pitää liuoksessa, yhdistyvät erikseen muodostaen kolloidisia hiukkasia.
kolloidisen liuoksen Puhdistus
dialyysi:
kolloidihiukkasten erottamista kristalloidihiukkasista diffuusion avulla sopivan kalvon (eläinkalvon tai pergamenttipaperin) läpi kutsutaan dialyysiksi. Dialyysissä käytettävää laitetta kutsutaan dialysaattoriksi.
periaate:
kolloidiset hiukkaset eivät pääse pergamentti-tai sellofaanikalvon läpi, kun taas elektrolyytin ionit (kristalloidit) voivat kulkea sen läpi.
prosessi:
kolloidiliuosta sisältävästä sopivasta puolipermeikkikalvosta koostuva pussi ripustetaan astiaan, jonka läpi makeaa vettä lennetään jatkuvasti. Kristalloidien molekyylit ja ionit diffuusioituvat kalvon läpi veteen ja huuhtoutuvat pois. Näin pussissa oleva sol puhdistetaan.
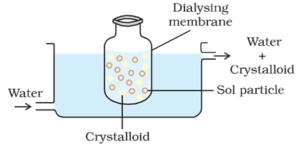
HCl voidaan poistaa ferrihydroksidisolista dialyysillä.
Elektrodialyysi:
tavallinen dialyysiprosessi on hidas. (ii) puhdistusprosessin lisäämiseksi dialyysi suoritetaan sähkökentän avulla. Tätä prosessia kutsutaan elektrodialyysiksi. Kolloidisessa liuoksessa olevat ionit siirtyvät kohti vastakkaisesti varautuneita elektrodeja.

tärkeä soveltaminen elektrodialyysin prosessi keinotekoinen munuaisten kone käytetään veren puhdistamiseen potilailla, joiden munuaiset eivät toimi.
ultrasuodatus:
tavallisen suodatinpaperin huokoset ovat suuret, joten kolloidiset hiukkaset läpäisevät ne helposti. Jos tavallisen suodatinpaperin huokosia pienennetään liottamalla suodatinpaperia kolloidioniliuoksessa (se on 4-prosenttisen nitroselluloosan seos alkoholissa ja eetterissä) ja sen jälkeen kovetetaan liottamalla formaldehydiin
, käsitelty suodatinpaperi voi säilyttää kolloidisia hiukkasia ja päästää todelliset liuoshiukkaset karkaamaan. Tällaista suodatinpaperia kutsutaan ultrasuodatukseksi ja kolloidien erottamisprosessi ultrasuodatinten avulla tunnetaan ultrasuodatuksena.
ultrasuodatinpaperille jääneet kolloidiset hiukkaset pestään sitten tuoreella dispersioväliaineella, jotta saadaan puhdas kolloidinen liuos.
Ultracentrifugaatio:
tässä menetelmässä kolloidinen liuos asetetaan suurnopeuslentopanssarikoneeseen. Sentrifugoinnissa kolloidiset hiukkaset laskeutuvat. Epäpuhtaudet jäävät sentrifugaattiin ja poistuvat. Vakiintuneet kolloidiset hiukkaset sekoitetaan dispersioaineeseen, jolloin kolloidinen liuos muodostuu uudelleen.